Por Carly Cassella
Publicado na ScienceAlert
Às vezes, a linha entre arte e ciência é tortuosa. Pesquisadores que estudam uma bactéria social que se move e se alimenta em enxames coordenados recriaram involuntariamente algo que se parece muito com uma obra-prima familiar.
Quando um determinado gene tem uma superexpressão em uma bactéria conhecida como Myxococcus xanthus, os organismos individuais se auto-organizam em minúsculos enxames circulares em poucas horas.
Uma vez que os enxames resultantes são coloridos artificialmente, a cena se parece muito com A Noite Estrelada de Van Gogh.
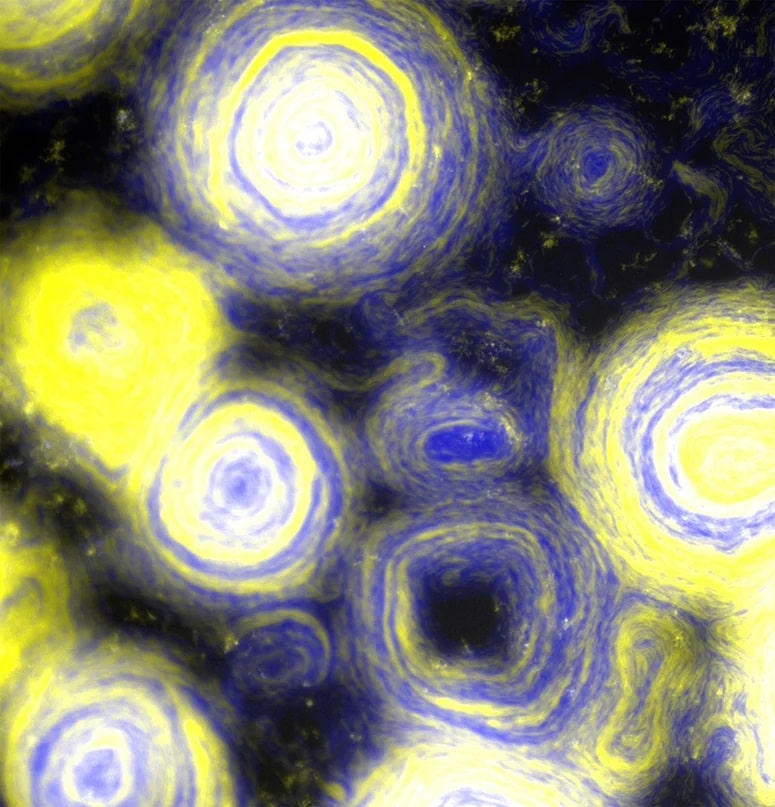
“Nosso trabalho destaca como uma bactéria social, conhecida por fontes ricas de produtos naturais terapêuticos e como agentes de biocontrole de cultivo, serve como um modelo poderoso para estudar comportamentos emergentes que também exibem beleza artística”, disse o microbiologista Daniel Wall, da Universidade de Wyoming.

As bactérias têm a reputação de serem egoístas, mas M. xanthus é descrita como uma bactéria social porque precisa encontrar e reconhecer familiares para sobreviver.
Depois de formar grandes aglomerados familiares, essa bactéria em forma de bastonete se torna muito melhor para atacar suas presas para se alimentar. Cada célula produz enzimas digestivas que facilitam a alimentação predatória.
Os pesquisadores estão fascinados por esse comportamento social há anos, mas ainda não temos um modelo abrangente e amplamente aceito para seus movimentos complexos.
Em 2017, Wall e seus colegas anunciaram a descoberta de uma única ‘chave’ genética responsável por ativar e desativar esse comportamento de agrupamento.
A chave controla especificamente uma sequência de proteína, conhecida como TraA, que fornece um receptor de superfície para a bactéria reconhecer e se ligar ao receptor parceiro, TraB, em seus parentes.
Depois de se colar a um membro da família por meio desses dois receptores (TraAB), a bactéria pode, então, trocar nutrientes e proteínas com o resto do grupo.
Quando o enxame encontra comida, pesquisas de laboratório mostram que os organismos podem realmente reunir suas enzimas e metabólitos por meio dessas conexões para dar golpes mais poderosos às suas presas.
Mas tudo isso muda quando a equipe induziu bactérias mutantes a superexpressar as conexões de TraAB. Essa conexão é o que permite que as células se unam em primeiro lugar, mas quando há muito dessa ‘cola social’, o enxame não consegue se separar tão facilmente para mudar sua forma ou direção.
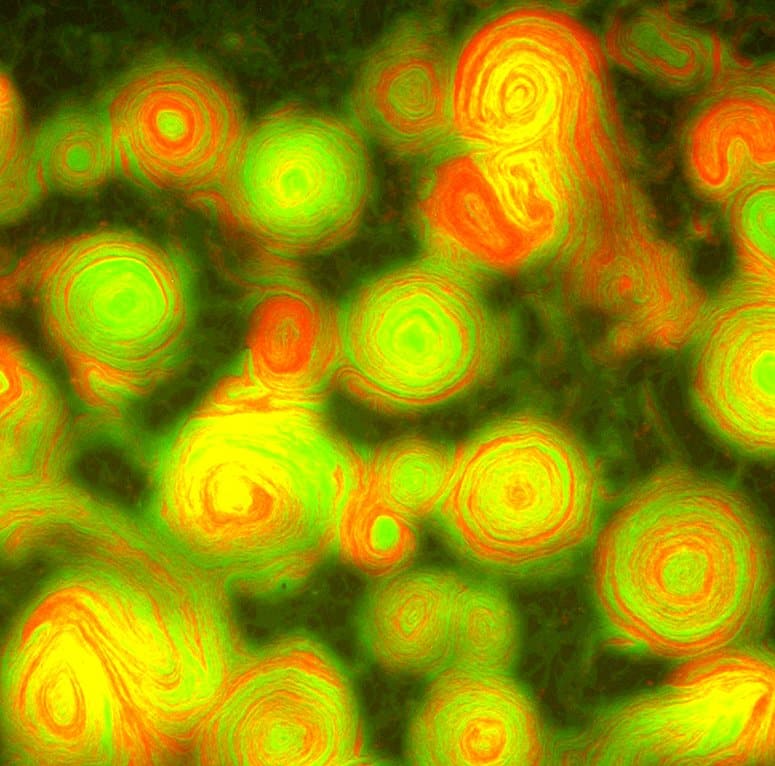
“Em células normais do tipo selvagem, eles vão e voltam, vão e vêm, como um trem de passageiros”, explicou o bioengenheiro Oleg Igoshin da Universidade Rice. “A cabeça se torna a cauda e a cauda se torna a cabeça. E eles fazem isso a cada 8 minutos ou mais”.
Uma superexpressão de TraAB, no entanto, parece impedir o enxame de mudar sua cabeça para sua cauda e vice-versa.
Isso é o que os modelos computacionais sugeriram que aconteceria, mas os autores ainda não conseguiram descobrir o porquê. Pelo que eles sabiam, a conexão de TraAB não estava diretamente envolvida na regulação dos movimentos do enxame, apenas sua aderência.
Em última análise, a equipe suspeitou que a característica pegajosa de TraB estava impedindo indiretamente o enxame de células de mudar de direção.
“Nossa ideia era que talvez houvesse algum tipo de sinal dependente do contato entre as células que suprime as reversões”, explicou Igoshin. “As células estão em grupos densos e estão em contato com outras o tempo todo, mas esses contatos são transitórios. Mas se a superexpressão de TraAB realmente o tornar pegajoso, seu vizinho continuará sendo seu vizinho por mais tempo, e isso pode disparar o sinal que suprime o reversões”.
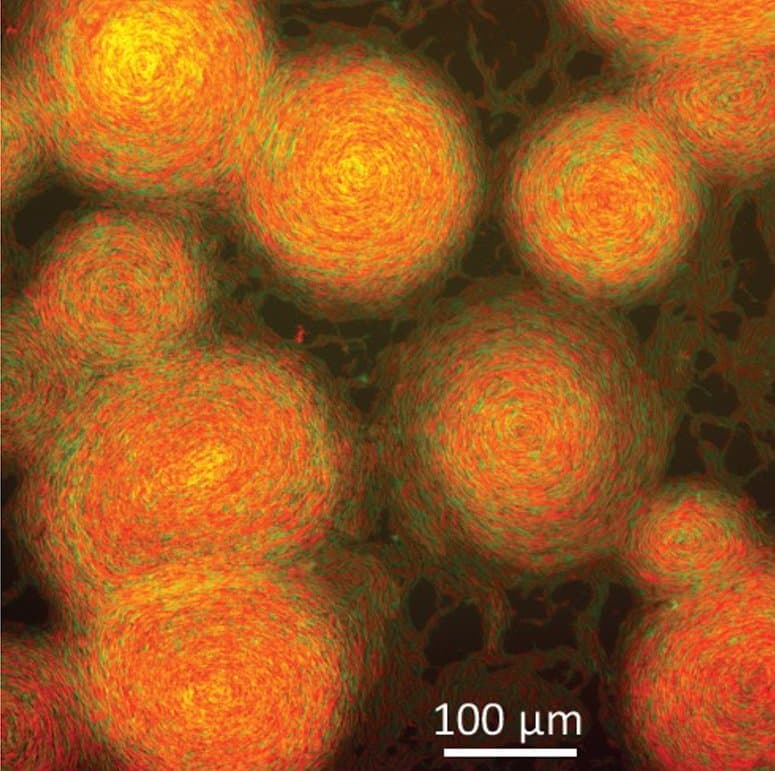
Rodando esse cenário em modelos computacionais, os autores puderam verificar seu palpite. Com apenas mudanças na conexão de TraAB, os enxames normais da cabeça à cauda de repente se tornaram redemoinhos giratórios de células, tão grandes quanto um milímetro ou mais.
Outros experimentos em laboratório confirmaram que isso também aconteceu com as bactérias na vida real. Especificamente, os redemoinhos podem ocorrer quando uma cepa superexpressa pegajosidade, mas também quando uma cepa é geneticamente modificada para ser diretamente ‘não reversível’.
O resultado não é apenas uma melhor compreensão de como milhões de células coordenam seus movimentos, mas também uma imagem hipnotizante do mundo microbiano.
O estudo foi publicado na mSystems.





