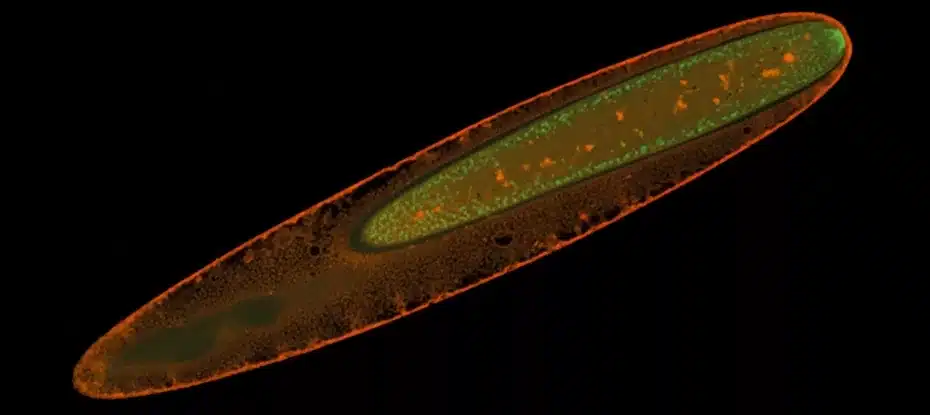
Pela primeira vez, os cientistas sequenciaram genomas de bactérias gigantes que pode ser vistas sem microscópio.
As descobertas sobre as suas estratégias reprodutivas, mecanismos de sobrevivência e mecanismos metabólicos distintos – semelhantes às mitocôndrias – poderão um dia ser úteis no desenvolvimento de tecnologias energéticas sustentáveis e no aumento da eficiência na agricultura.
A bactéria Epulopiscium vive simbioticamente nas entranhas de um peixe, Naso tonganus, em ambientes oceânicos tropicais. Enquanto a maioria das bactérias são muito pequenas para serem vistas sem um microscópio, estes mamutes unicelulares têm um milhão de vezes o volume dos seus parentes bem conhecidos, a E. coli, o que significa que ser vistos a olho nu.
“Esta incrível bactéria gigante é única e interessante em muitos aspectos”, diz a microbiologista Esther Angert, da Universidade Cornell, nos EUA. “Revelar o potencial genômico deste organismo simplesmente nos surpreendeu.”
O primeiro membro do Epulopiscium – cujo nome vem das palavras latinas para “um convidado” e “de um peixe” – foi descoberto em 1985.
Angert e os seus colegas norte-americanos nomearam a espécie que estudaram como Epulopiscium viviparus: A segunda palavra refere-se à reprodução que resulta em nascimentos vivos.
Embora as bactérias normalmente se dividam ao meio para formar duas novas, o E. viviparus pode fazer até 12 cópias de si mesmo dentro da célula-mãe.

Incapazes de serem cultivadas em laboratório, essas bactérias gigantes continuam sendo uma curiosidade do mundo biológico. Portanto, para estudar o E. viviparus, os pesquisadores tiveram que capturar os peixes em que ele vive e coletar cuidadosamente as células o mais rápido possível para sequenciamento de DNA e análise do transcriptoma.
A maioria das bactérias respira usando oxigênio ou obtém energia do ambiente por meio de fermentação, o que geralmente resulta em menor produção de energia.
E. viviparus é um fermentador, mas isso é intrigante porque é enorme, se reproduz rapidamente e pode nadar – tudo isso exigindo quantidades relativamente grandes de energia.
Parece que as bactérias otimizaram o seu metabolismo para um ambiente intestinal de peixe rico em íons de sódio. O fluxo de íons de sódio através das membranas celulares gera uma poderosa “força motriz de sódio” para produzir energia e girar seus apêndices semelhantes a cabelos, chamados flagelos, para o movimento.
Esta força motriz do sódio também alimenta o movimento dos flagelos no Vibrio cholerae, a bactéria que causa a cólera.
A equipe também descobriu que uma grande parte do código genético do E. viviparus produz enzimas que são altamente eficientes na extração de nutrientes dos peixes hospedeiros, especialmente carboidratos chamados polissacarídeos das algas que constituem grande parte da dieta do N. tonganus
E. viviparus possui enzimas abundantes que também produzem ATP, a “moeda energética” que suporta uma ampla variedade de processos celulares. Eles descobriram espaço para essas moléculas em uma membrana única, semelhante às mitocôndrias de organismos mais complexos.
“Todos nós conhecemos a frase “as mitocôndrias são a força motriz da célula” e, surpreendentemente, essas membranas em E. viviparus convergiram para o mesmo modelo das mitocôndrias”, diz Angert.
“Eles têm uma membrana altamente dobrada que aumenta a área de superfície onde essas bombas produtoras de energia podem funcionar, e esse aumento na área de superfície cria uma usina de energia.”
As formas eficientes do E. viviparus de aproveitar os nutrientes das algas podem ter muitos usos no futuro. As algas estão tornando-se mais populares como fonte de energia renovável, fonte de alimento para o gado e também para as pessoas, porque o seu crescimento não interfere na agricultura terrestre.
Ainda existem alguns mistérios a serem resolvidos. Como apontam Angert e colegas, são necessários mais estudos para compreender completamente como o E. viviparus utiliza o seu arsenal de enzimas. Mas isto fornece uma base sólida para a compreensão das suas necessidades de crescimento.
“Achamos notável que as maiores bactérias conhecidas tenham até agora escapado ao isolamento”, escrevem os autores. “Isso sugere que os gigantes bacterianos estão altamente preparados para sobreviver nos ambientes em que evoluíram.”
Publicado em ScienceAlert
Traduzido por Mateus Lynniker