Transformar dióxido de carbono em insumos úteis continua sendo uma das apostas mais sérias da química aplicada ao clima. O desafio não é pequeno. Não basta capturar o CO2, é preciso fazê-lo reagir de forma seletiva, estável e economicamente viável. É justamente nesse ponto que um novo desenho de eletrodo chama atenção. Em vez de apenas tentar empurrar a reação com mais energia, a equipe da KAIST redesenhou a própria arquitetura do material para resolver um gargalo conhecido, o flooding, quando o eletrólito invade os poros do eletrodo e derruba o desempenho. O resultado foi um sistema mais durável e mais eficiente para converter CO2 em compostos de carbono mais complexos, incluindo etileno, um precursor importante da indústria de plásticos.
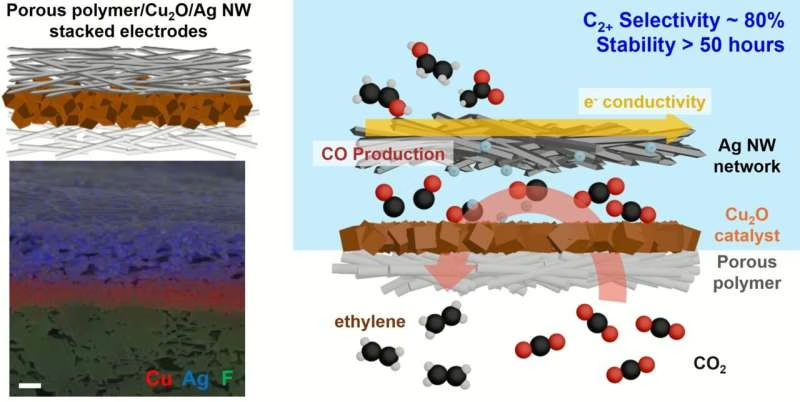
De acordo com o estudo publicado na Advanced Science, o eletrodo combina três camadas com funções distintas. A base é um substrato hidrofóbico, pensado para bloquear a entrada de água. Sobre ele, os pesquisadores colocaram uma camada catalítica de óxido de cobre. Na parte superior, uma rede de nanofios de prata atua como coletor de corrente e, ao mesmo tempo, participa ativamente da reação. Essa combinação evita a simplificação enganosa de que um eletrodo bom é apenas aquele que conduz bem. Aqui, a eficiência nasce da cooperação entre estrutura física, transporte de carga e catálise.
O ponto mais interessante é que os nanofios de prata não ficaram restritos ao papel de condutores. Eles produziram monóxido de carbono durante a redução eletroquímica do CO2, e esse intermediário foi então transferido para os catalisadores à base de cobre, onde novas etapas reacionais ocorreram. Em termos práticos, isso cria um sistema tandem, no qual dois componentes trabalham em sequência para empurrar a química até produtos com mais átomos de carbono. Esse tipo de desenho interessa porque a formação de moléculas C2+ costuma ser mais difícil do que gerar produtos simples, mas é justamente ela que aponta para um uso industrial mais valioso.
A eficiência anunciada, 86% em eletrólitos neutros, não é um detalhe de marketing. Ela significa que a maior parte da corrente elétrica aplicada foi convertida no produto desejado. Em eletrólitos alcalinos, o sistema também se saiu muito bem, com 79% de seletividade para produtos C2+. Para completar, o eletrodo manteve operação estável por mais de 50 horas sem perda relevante de desempenho. Isso importa porque tecnologias de conversão de carbono costumam tropeçar em dois problemas ao mesmo tempo, baixa seletividade e pouca durabilidade. Resolver um sem o outro costuma gerar demonstrações elegantes, mas pouco úteis fora do laboratório.
A relevância dessa notícia cresce quando ela sai do vocabulário de bancada e entra no contexto da descarbonização industrial. Ethylene é um dos blocos mais importantes da petroquímica global e está na base de uma longa cadeia de materiais, inclusive plásticos. Se o CO2 puder ser transformado com boa eficiência em moléculas intermediárias úteis, abre-se uma rota para usar carbono de origem residual como matéria-prima. Isso não elimina a necessidade de reduzir emissões na origem, mas pode integrar captura e uso de carbono em processos industriais mais circulares. A aposta aqui não é em milagre tecnológico, e sim em engenharia química refinada.
Esse tipo de avanço também ajuda a corrigir uma ideia simplista que costuma aparecer em debates sobre carbono. Não basta perguntar se uma tecnologia “captura CO2”. É preciso perguntar se ela captura, converte, sustenta operação por tempo suficiente e produz algo com valor real. Sem esses quatro elementos, a solução fica presa na categoria de protótipo promissor. A nova arquitetura da KAIST é interessante justamente porque tenta responder a essas quatro perguntas ao mesmo tempo. Ela bloqueia o flooding, mantém condutividade, favorece reações em cascata e sustenta desempenho por tempo razoável. Isso é mais sólido do que promessas abstratas de química verde.
Também vale notar que a lógica do estudo conversa com outras fronteiras da ciência dos materiais. Em vez de confiar em uma única função para cada componente, os pesquisadores exploram materiais multifuncionais, capazes de conduzir, catalisar e estruturar o ambiente reacional. Essa lógica já aparece em outras áreas, como mostramos em Em processo inovador cientistas produziram diamantes em 150 minutos, onde o controle do ambiente de reação é decisivo para obter o material desejado. O mesmo raciocínio aparece em Cientistas desenvolveram uma nova maneira de observar cristais, que mostra como novas ferramentas mudam o que conseguimos enxergar nos materiais. Em química aplicada, às vezes a grande virada não está na molécula final, mas na maneira como ela é produzida.
O estudo não resolve sozinho o problema climático nem transforma CO2 em solução mágica para a indústria do plástico. Contudo, ele mostra algo mais valioso. Mostra que a rota da conversão eletroquímica está amadurecendo, com ganhos concretos em seletividade, estabilidade e desenho racional de materiais. Em um campo cheio de promessas vagas, esse tipo de resultado tem peso porque oferece números, mecanismo e um caminho técnico plausível. Se a próxima etapa confirmar escalabilidade e custo compatível, a conversão de CO2 pode deixar de ser uma ideia bonita e passar a ocupar um lugar real na química industrial do século 21.