Graças em parte ao tamanho do átomo, uma variação carregada de ouro chamada Au 2+ não é comumente encontrada na natureza.
Cientistas da Universidade de Stanford, da Universidade da Califórnia, Berkeley, e da Universidade McGill, no Canadá, conseguiram agora criar e estabilizar o íon raro, permitindo uma série de novos usos para este fascinante metal elementar.
Os átomos de ouro têm muitos prótons agrupados em seus núcleos, o que lhes confere uma grande carga positiva que atrai com força os elétrons em órbita. Estas forças invulgarmente fortes tornam os efeitos da relatividade especial na sua aceleração muito mais significativos, tornando alguns arranjos de elétrons mais prováveis do que outros.
Esta configuração relativística não só confere ao ouro o seu brilho amarelado, como também torna a perda de um ou três elétrons mais provável do que a perda de dois.
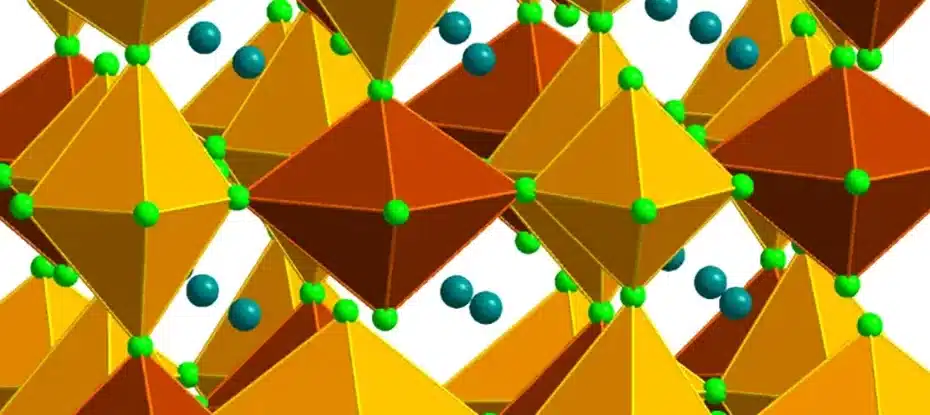
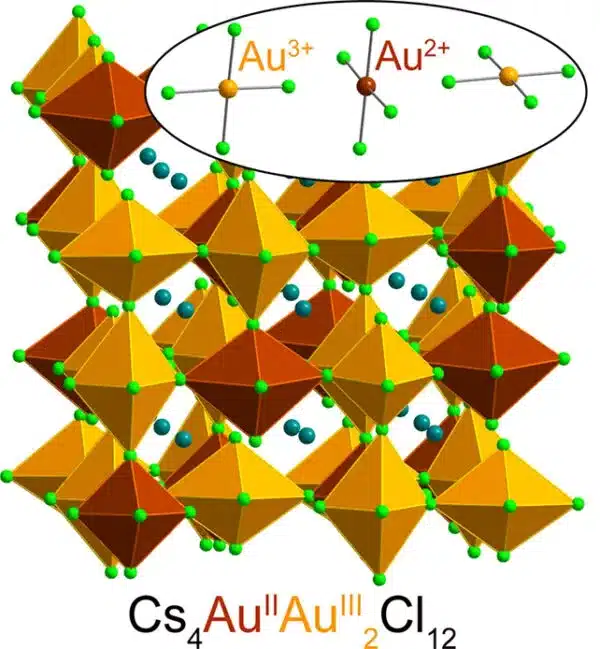
Aqui, os químicos capturaram íons de ouro em um tipo de material cristalino chamado perovskita haleto, que é usado em todos os lugares, desde painéis solares até dispositivos eletrônicos.
A configuração especial dos elementos no cristal estabilizou quaisquer íons Au 2+ que se formaram dentro de sua matriz, preservando efetivamente seu estado único.
“As perovskitas haleto possuem propriedades realmente atraentes para muitas aplicações cotidianas, por isso procuramos expandir esta família de materiais”, diz o químico Kurt Lindquist, anteriormente na Universidade de Stanford e agora na Universidade de Princeton.
“Uma perovskita Au 2+ sem precedentes poderia abrir alguns novos caminhos intrigantes.”
Descoberta como parte de uma pesquisa separada sobre semicondutores magnéticos e como eles podem melhorar dispositivos eletrônicos, a fórmula inclui uma mistura de sal de cloreto de césio, cloreto de Au 3+, água, ácido clorídrico e “um pouco de vitamina C”.
“No laboratório, podemos fazer este material utilizando ingredientes muito simples em cerca de cinco minutos à temperatura ambiente”, diz Lindquist.
“Acabamos com um pó verde muito escuro, quase preto, e surpreendentemente pesado devido ao ouro que contém.”
Ao doar um de seus elétrons, a vitamina C transforma o íon Au 3+ em Au 2+. Diversas análises confirmaram que os cientistas tinham de fato produzido o mais raro dos estados de ouro numa forma estável.
O ouro é um elemento atraente por vários motivos, além de sua cor bastante atraente: é relativamente fácil de remodelar, mas não reage facilmente com outros produtos químicos, o que significa que não mancha nem se degrada com o tempo.
Agora que temos uma forma nova e estável para usar, os próximos passos são examinar mais de perto as características ópticas e eletrônicas do Au 2+, características que poderiam eventualmente ser ajustadas e usadas na eletrônica e em outros campos.
“Foi uma verdadeira surpresa termos conseguido sintetizar um material estável contendo Au 2+ – a princípio nem acreditei”, diz o químico Hemamala Karunadasa, da Universidade de Stanford.
“Estamos entusiasmados em explorar o que uma perovskita Au 2+ poderia fazer.”
Traduzido por Mateus Lynniker de ScienceAlert