Traduzido por Julio Batista
Original de Emily Swaim para o Business Insider
Por milênios, os humanos têm tentado estender nossa expectativa de vida o máximo que podem. Tentamos congelar nossos organismos, jejuar e usar remédios à base de ervas em abundância.
Recentemente, bilionários como Larry Page, Mark Zuckerberg e Jeff Bezos investiram fortemente em empresas de biotecnologia como Altos Labs, Juvenescence e Unity Biotechnology, que buscam a longevidade por meio do rejuvenescimento celular e prevenção de doenças.
Até agora, o tempo mais longo que sabemos que alguém já viveu foi 122 anos. Mas isso pode estar no limite inferior do nosso limite potencial.
Os seres humanos podem ter um limite de vida de 150 anos
Mesmo se você vivesse em uma bolha sem doenças ou perigos, seu corpo ainda experimentaria desgaste ao bombear sangue, digerir comida e conduzir todas as funções necessárias para a sobrevivência.
Quanto mais você envelhece, mais tempo levará para o seu corpo “se recuperar” desse desgaste, porque o envelhecimento está embutido em nossas células e DNA. Tudo isso significa que seus tecidos perdem gradualmente a capacidade de se curar, o que pode levar a doenças e disfunções.
Um estudo sugeriu que o tempo de recuperação do corpo humano dobra a cada 15 anos – portanto, uma contusão que levou uma semana para cicatrizar aos 40 anos pode levar duas semanas aos 55 anos. Eventualmente, o corpo humano perde toda a sua resiliência, então quaisquer ossos ou tecidos quebrados permanecem quebrados. Uma vez que muitas partes do corpo funcionam mal, você morre.
Os pesquisadores não concordam necessariamente com o limite máximo para quando isso acontece. Alguns propuseram 115 anos, outros 130 anos. Um dos estudos mais recentes analisando mais de meio milhão de pessoas nos Estados Unidos e no Reino Unido sugeriu que os humanos perdem toda a resiliência em algum momento entre 120 e 150 anos.
A grande questão é: e se pudéssemos retardar esse desgaste, ou melhor ainda, evitá-lo completamente? Alguns especialistas argumentam que, com os avanços médicos, a expectativa de vida humana média não tem limite natural.
Olhando no envelhecimento em nível celular para ver o que está nos impedindo de ter uma vida mais longa, grupos de pesquisadores procuram entender e potencialmente reverter o processo de envelhecimento.
A senescência celular é um dos tópicos mais pesquisados do envelhecimento
A senescência celular é quando uma célula para de se reproduzir, mas não morre.
Quando isso acontece, algumas células senescentes se transformam em zumbis destrutivos, flutuando e liberando substâncias químicas inflamatórias que prejudicam células saudáveis, incluindo células-tronco – os “reparadores” do seu corpo que ajudam a substituir tecidos danificados ou quebrados.
Mas nem todas as células senescentes são ruins.
Algumas células senescentes secretam substâncias químicas que ajudam a reparar feridas, disse Paul Robbins, diretor associado do Instituto de Biologia do Envelhecimento e Metabolismo e da Equipe de Descobertas Médicas em Biologia do Envelhecimento da Universidade de Minnesota, EUA.
Empresas como Life Biosciences e Unity Biotechnology estão atualmente desenvolvendo drogas chamadas senolíticas para conter e destruir apenas as células senescentes “ruins” em seu corpo. Algumas drogas experimentais podem até impedir que as células se tornem senescentes em primeiro lugar.
Mas até agora, ninguém descobriu como prevenir ou eliminar completamente as células senescentes nocivas.
Aos 60 anos, o corpo humano – em particular o sistema imunológico – tem mais dificuldade em eliminar as células senescentes nocivas, o que pode levar a um acúmulo que desencadeia danos e falhas nos tecidos, disse Robbins.
Uma das principais causas da senescência celular é o dano ao seu DNA , que ajudou a desencadear outra área de pesquisa que levou ao Prêmio Nobel em 2009: os telômeros.
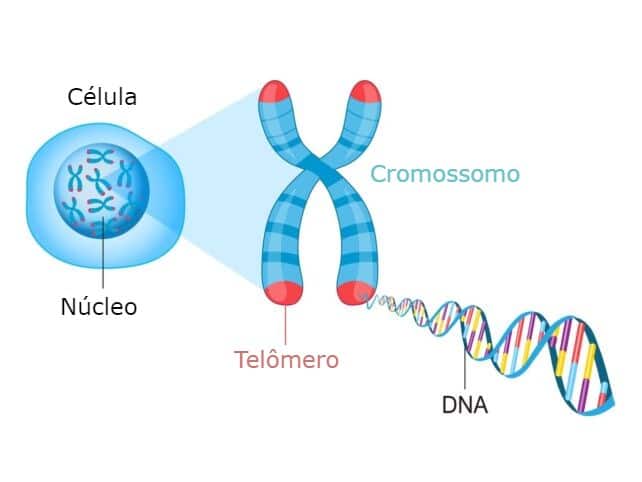
Os telômeros ajudam a estimar sua idade biológica
Alguns argumentam que a idade biológica – a idade de suas células e tecidos – é um indicador melhor de sua expectativa de vida do que sua idade cronológica, ou quantos anos você está vivo.
Uma maneira comum dos cientistas estimarem a idade biológica é medir os telômeros em certas células imunológicas.
Os telômeros são tampas protetoras no final do seu DNA. Eles são feitos de cadeias de moléculas chamadas pares de bases. Conforme você envelhece, esses pares de bases desaparecem, encurtando seus telômeros. E telômeros mais curtos deixam o DNA mais vulnerável a danos e aos efeitos do envelhecimento.
Quando você nasce, os telômeros de certas células imunológicas, chamadas leucócitos, podem ter entre 7.000 e 11.600 pares de bases. Uma vez que esse tamanho diminui para 5.000 pares de bases, você corre um alto risco de morte iminente, segundo um estudo recente.
Mas outra pesquisa descobriu que algumas pessoas que vivem mais de 100 anos realmente experimentam telômeros que ficam mais longos a cada ano, não mais curtos. Isso levou alguns cientistas a pesquisar maneiras de imitar esse processo de recuperação dos telômeros em indivíduos mais jovens.
Por exemplo, a Aviv Clinics realizou um estudo examinando como 35 adultos mais velhos responderam à oxigenoterapia hiperbárica, na qual você descansa em uma câmara com alta pressão de ar e níveis de oxigênio. Eles conseguiram aumentar o comprimento dos telômeros nas células leucocitárias dos participantes após 30 sessões diárias de OHB.
Mas a maioria dos telômeros parou de crescer após a 30ª sessão, e os cientistas ainda não sabem quanto tempo os efeitos do tratamento podem durar.
A metilação do DNA está ligada a várias doenças relacionadas à idade
Outro contribuinte para danos ao DNA e senescência celular é a metilação do DNA – quando moléculas chamadas grupos metila se ligam a certas seções de seus genes para controlar seu comportamento.
Dependendo da localização, os grupos metila podem bloquear a ativação dos genes ou aumentar a atividade dos genes quando necessário.
Em geral, a metilação do DNA diminui à medida que você envelhece, o que pode permitir a ativação dos genes errados.
A pesquisa ligou o declínio da metilação a várias condições relacionadas à idade, incluindo doença de Alzheimer, doenças cardiovasculares e câncer – embora seja importante notar que nem todas as alterações de metilação são ruins.
Semelhante aos telômeros, a metilação do DNA é outra maneira pela qual os cientistas podem medir sua idade biológica para ajudar a prever sua expectativa de vida. Por exemplo, você pode ter comemorado seu aniversário de 55 anos, mas depois de anos fumando, suas células podem ter um nível de metilação geralmente visto em pessoas de 60 anos, encurtando potencialmente sua vida útil.
Tradicionalmente, os testes de metilação do DNA usam sangue, mas empresas como a Elysium Health e projetos de pesquisa como o GrimAge também desenvolveram recentemente testes de saliva.
As pessoas cuja idade de metilação é pelo menos 5 anos maior que sua idade cronológica têm um risco de mortalidade 16% maior, segundo a pesquisa, o que significa que são mais propensas a morrer por diversas causas relacionadas a saúde do que seus pares da mesma idade.
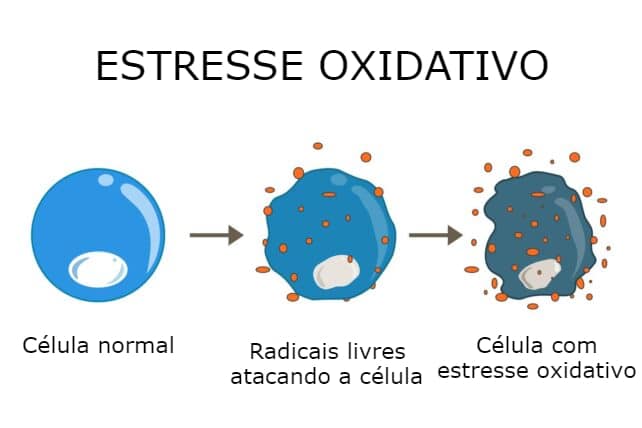
As mitocôndrias e os radicais livres são alguns dos maiores obstáculos à longevidade
Por último, mas não menos importante, alguns dos maiores limitadores da vida humana são as minúsculas mitocôndrias em forma de feijão em suas células. Essas estruturas microscópicas geram a maior parte da energia de uma célula, que é vital para a sobrevivência, mas também cria subprodutos chamados radicais livres.
Os radicais livres são basicamente átomos instáveis que saltam e danificam partes de sua célula, levando a danos chamados de estresse oxidativo. Com o tempo, o estresse oxidativo se acumula, causando doenças relacionadas à idade, como Parkinson, Alzheimer e câncer.
Empresas de biotecnologia como Altos Labs estão trabalhando em uma maneira de prevenir essas doenças, rejuvenescendo as células e desfazendo os danos que o estresse oxidativo pode causar. A empresa espera que, ao redefinir as células para um estado mais jovem e saudável, isso possa aumentar a longevidade.
A busca pela longevidade não tem uma solução única
Para cada mecanismo que contribui para o envelhecimento, existem grupos de pessoas trabalhando para entender e possivelmente reverter esses processos.
Mas é importante observar que o quebra-cabeça do envelhecimento não tem uma solução única.
“Todas essas coisas ruins que surgem com o envelhecimento estão ligadas”, disse Robbins.
Por exemplo, o encurtamento dos telômeros pode levar a danos no DNA, o que, por sua vez, prejudica suas mitocôndrias. Os radicais livres de suas mitocôndrias podem, por sua vez, danificar mais de seus telômeros e DNA. Todos esses processos se influenciam mutuamente.
Nenhum mecanismo de envelhecimento é mais importante que os outros. É por isso que toda pesquisa antienvelhecimento, não importa o nicho, é uma parte conectada do objetivo maior da humanidade: permanecer vivo o máximo que pudermos.