Por Mindy Weisberger
Publicado na Live Science
O que acontece quando você pega células de embriões de sapos e transforma em novos organismos “evoluídos” por algoritmos? Você obtém algo que os pesquisadores chamam de primeiro “robô vivo” do mundo.
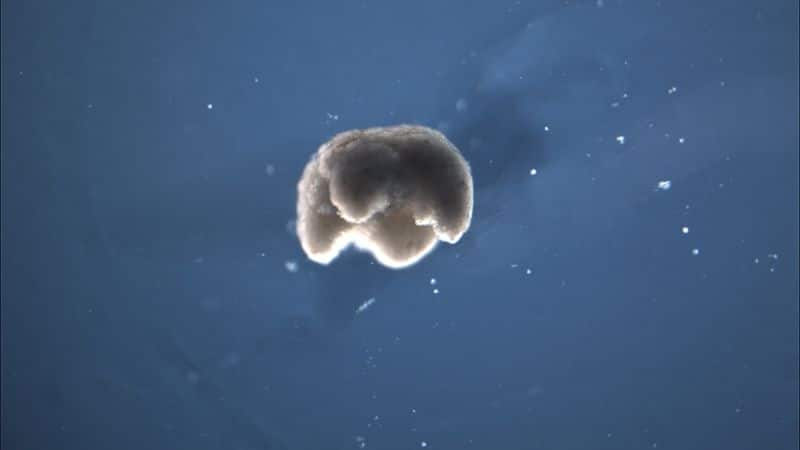
Embora as células-tronco originais venham de sapos – o sapo com garras africanas, Xenopus laevis – esses chamados xenobots não se parecem com nenhum anfíbio conhecido. As pequenas bolhas medem apenas 1 milímetro de largura e são feitas de tecido vivo, que os biólogos reuniram em corpos projetados por um programa de computador, de acordo com um novo estudo.
Esses organismos móveis podem se mover de forma independente e coletiva, curar feridas e sobreviver por semanas seguidas e, potencialmente, podem ser utilizados para transportar medicamentos dentro do corpo de um paciente.
“Eles não são um robô tradicional e nem uma espécie conhecida de animal”, afirmou o coautor do estudo, Joshua Bongard, cientista da computação e especialista em robótica da Universidade de Vermont. “É uma nova classe de artefato: um organismo vivo e programável”.
Algoritmos moldaram a evolução dos xenobots. Eles cresceram de células-tronco da pele e do coração para grupos de centenas de células que se moviam em pulsos gerados pelo tecido muscular do coração, disse o principal autor do estudo, Sam Kriegman, um candidato a doutorado que estuda robótica evolutiva no Departamento de Ciência da Computação da Universidade de Vermont, em Burlington.
“Não há controle externo a partir de um controle remoto ou bioeletricidade. Esse é um agente autônomo – é quase como um brinquedo de corda”, disse Kriegman à Live Science.
Os biólogos aumentaram as restrições dos xenobots autônomos a partir de um programa de computador, como a potência muscular máxima de seus tecidos e como eles podem se mover em um ambiente aquoso. Então, o algoritmo produziu gerações de minúsculos organismos. Os robôs com melhor desempenho “se reproduziam” dentro do algoritmo. Assim como a evolução funciona no mundo natural, as formas menos bem-sucedidas seriam excluídas pelo programa de computador.
“Eventualmente, ele foi capaz de nos fornecerem projetos que eram realmente transferíveis para células reais. Isso foi um avanço”, disse Kriegman.
Os autores do estudo trouxeram à vida esses desenhos, reunindo células-tronco para elaborar formas 3D autoalimentadas projetadas pelo algoritmo de evolução. As células da pele mantinham os xenobots unidos e o batimento do tecido cardíaco em partes específicas de seus “corpos” impulsionava os robôs pela água em uma placa de Petri por dias e até semanas seguidas, sem a necessidade de nutrientes adicionais, de acordo com o estudo. Os robôs conseguiram até reparar danos significativos, disse Kriegman.
“Cortamos o robô vivo quase pela metade e suas células fecharam automaticamente o corpo”, disse ele.
“Podemos imaginar muitas aplicações úteis desses robôs vivos do que outras máquinas não podem fazer”, disse o coautor do estudo, Michael Levin, diretor do Centro de Biologia Regenerativa e do Desenvolvimento da Universidade Tufts, em Massachusetts. Isso pode incluir reparar derramamentos tóxicos ou contaminação radioativa, coletar microplásticos marinhos ou até escavar placas de artérias humanas, disse Levin em comunicado.
A perspectiva da criação dos chamados robôs vivos – e o uso da tecnologia para criar organismos vivos – suscita compreensivelmente preocupações de especialistas, disse Levin.
“Esse medo não é irracional”, disse Levin. “Quando começarmos a mexer com sistemas complexos que ainda não entendemos, teremos consequências não intencionais”. No entanto, desenvolver formas orgânicas simples, como os xenobots, também pode levar a descobertas benéficas, acrescentou.
“Se a humanidade sobreviver no futuro, precisaremos entender melhor como propriedades complexas emergem de elementos mais simples”, disse Levin.
Os resultados do estudo foram publicados na revista Proceedings da National Academy of Sciences.