Por Nick Norman
Publicado no The Conversation
A tabela periódica dos elementos químicos, criada principalmente pelo químico russo Dmitri Mendeleiev (1834-1907), completou 150 anos no ano passado. Seria difícil não exaltar sua importância como princípio organizador na química – todos os químicos em formação se familiarizam com ela desde os primeiros estágios de sua educação.
Dada a importância da tabela, alguém pode ser perdoado por pensar que a ordem dos elementos não estava mais sujeita a debate. No entanto, dois cientistas em Moscou, Rússia, publicaram recentemente uma proposta para uma nova organização.
Vamos primeiro considerar como a tabela periódica foi desenvolvida. No final do século 18, os químicos faziam uma clara distinção entre um elemento e um composto: os elementos eram quimicamente indivisíveis (exemplos são hidrogênio, oxigênio) enquanto os compostos consistiam em dois ou mais elementos combinados, com propriedades bastante distintas de seus elementos componentes.
No início do século 19, havia boas evidências circunstanciais da existência de átomos. E na década de 1860, era possível listar os elementos conhecidos em ordem de sua massa atômica relativa – por exemplo, o hidrogênio era 1 e o oxigênio 16.
Listas simples, é claro, são unidimensionais por natureza. Mas os químicos estavam cientes de que certos elementos tinham propriedades químicas bastante semelhantes: por exemplo, lítio, sódio e potássio ou cloro, bromo e iodo.
Algo parecia se repetir e ao colocar elementos quimicamente semelhantes próximos uns dos outros, uma tabela bidimensional poderia ser construída. E assim, a tabela periódica nasceu.
É importante ressaltar que a tabela periódica de Mendeleiev foi derivada empiricamente com base nas semelhanças químicas observadas de certos elementos. Somente no início do século 20, depois que a estrutura do átomo foi estabelecida e seguindo o desenvolvimento da teoria quântica, uma compreensão teórica de sua estrutura surgiria.
Os elementos agora eram ordenados pelo número atômico (o número de partículas carregadas positivamente chamadas prótons no núcleo atômico), em vez da massa atômica, mas ainda por semelhanças químicas.
Essa última agora resultava do arranjo de elétrons que se repetiam nas chamadas “camadas” em intervalos regulares. Na década de 1940, a maioria dos livros didáticos apresentava uma tabela periódica semelhante às que vemos hoje, conforme mostrado na figura abaixo.
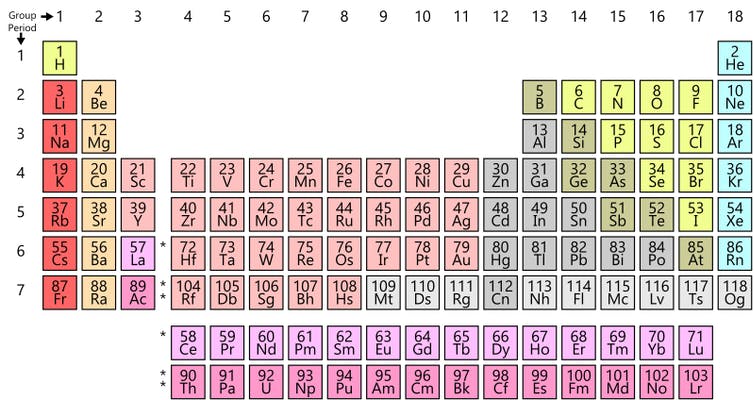
Seria compreensível pensar que isso encerraria o assunto. Mas não é bem assim, entretanto. Uma simples pesquisa na Internet revelará todos os tipos de versões da tabela periódica.
Existem versões curtas, versões longas, versões circulares, versões espirais e até versões tridimensionais. Muitas delas, com certeza, são simplesmente maneiras diferentes de transmitir a mesma informação, mas continua a haver desacordo sobre onde alguns elementos devem ser colocados.
O posicionamento preciso de certos elementos depende de quais propriedades particulares desejamos destacar. Assim, uma tabela periódica que dá primazia à estrutura eletrônica dos átomos será diferente das tabelas para as quais os critérios principais são certas propriedades químicas ou físicas.
Essas versões não diferem muito, mas existem certos elementos – hidrogênio, por exemplo – que podemos colocar de forma bem diferente de acordo com a propriedade particular que se deseja destacar. Algumas tabelas colocam o hidrogênio no grupo 1, enquanto em outras ele fica no topo do grupo 17; algumas tabelas até o possuem em um grupo próprio.
De uma forma mais radical, entretanto, podemos também considerar ordenar os elementos de uma maneira muito diferente, uma que não envolva número atômico ou se relacione a estrutura eletrônica – revertendo para uma lista unidimensional.
Nova proposta
A última tentativa de ordenar os elementos dessa maneira foi publicada recentemente no Journal of Physical Chemistry pelos cientistas Zahed Allahyari e Artem Oganov.

Sua abordagem, baseada no trabalho anterior de outros cientistas, é atribuir a cada elemento o que é chamado de Número de Mendeleiev (NM).
Existem várias maneiras de derivar esses números, mas o estudo mais recente usa uma combinação de duas grandezas fundamentais que podem ser medidas diretamente: o raio atômico de um elemento e uma propriedade chamada eletronegatividade, que descreve a força com que um átomo atrai elétrons para si mesmo.
Se alguém ordena os elementos por seu NM, os vizinhos mais próximos têm, como era de se esperar, NMs semelhantes. Porém, mais útil é dar um passo adiante e construir uma grade bidimensional baseada no NM dos elementos constituintes nos chamados “compostos binários”.
São compostos com composição de dois elementos, como o cloreto de sódio, NaCl.
Qual é a vantagem dessa abordagem? É importante ressaltar que ela pode ajudar a prever as propriedades de compostos binários que ainda não foram feitos. Isso é útil na busca de novos materiais que provavelmente serão necessários para tecnologias futuras e existentes. Com o tempo, sem dúvida, isso será estendido a compostos com mais de dois componentes elementares.
Um bom exemplo da importância da busca por novos materiais pode ser apreciado considerando a tabela periódica mostrada na figura abaixo.
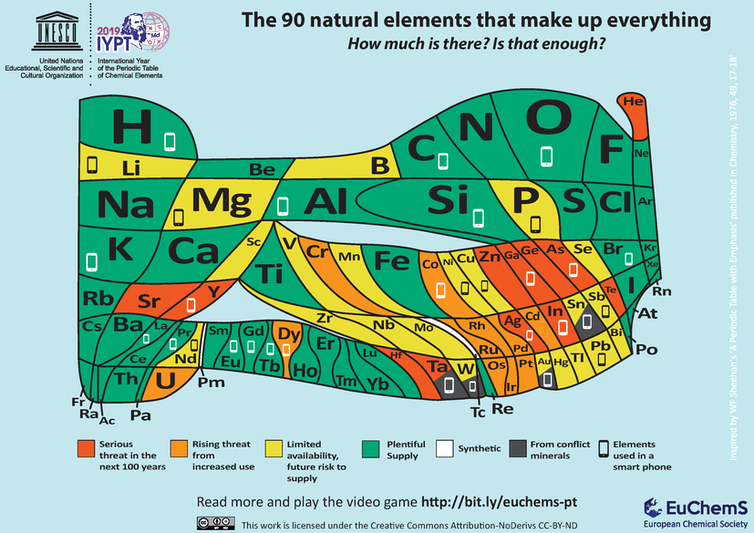
Esta tabela ilustra não apenas a abundância relativa dos elementos (quanto maior a caixa para cada elemento, mais há disponível), mas também destaca os problemas de abastecimento potenciais relevantes para tecnologias que se tornaram onipresentes e essenciais em nossas vidas diárias.
Pegue por exemplo os telefones celulares. Todos os elementos usados em sua fabricação são identificados com o ícone do telefone e você pode ver que vários elementos necessários estão se tornando escassos – seu fornecimento futuro é incerto.
Se quisermos desenvolver materiais de reposição que evitem o uso de certos elementos, essas perspectivas obtidas ao organizar elementos por seu NM podem ser valiosos nessa pesquisa.
Depois de 150 anos, podemos ver que as tabelas periódicas não são apenas uma ferramenta educacional vital, elas permanecem úteis para os pesquisadores em sua busca por novos materiais essenciais. Mas não devemos pensar em novas versões como substitutos de representações anteriores. Ter muitas tabelas e listas diferentes serve apenas para aprofundar nossa compreensão de como os elementos se comportam.